кальций при онкологии какой
Кальций при онкологии какой
Повышенный уровень кальция в плазме часто сопровождает рак. В госпитале к самым общим зловредным причинам гиперкальциемии относится рак бронхов, молочной железы и почек вместе с множественной миеломой. Угрожающая жизни гиперкальциемия обычно возникает из-за рака. Небольшие отклонения в концентрации кальция в плазме (до 2,8 ммоль/л) обычно не ассоциируются с какими-либо симптомами.
Как только концентрация кальция в плазме увеличивается, у пациентов появляются потеря аппетита, тошнота, абдоминальная боль, запор и усталость. Могут возникнуть мышечная слабость, полиурия и полидипсия. Иногда с увеличивающейся гиперкальциемией происходит серьезная дегидратация, потеря сознания и в конечном итоге кома.
Костные метастазы — наиболее частые причины гиперкальциемии при раке. Большинство пациентов с серьезной гиперкальциемией имеют метастазы, доказуемые при радиографии или при сканировании кости. Аспирация костного мозга может показать наличие опухоли.
Даже если метастазы не обнаруживаются при анализе, они обычно быстро становятся видимыми. Метастазы в кости стимулируют активность остеобластов локальным выделением белка, родственного паратиреоидному гормону (РТНгР).
К маркерам костной резорбции относятся трансформирующий ростовой фактор (TGF-a, TGF-P), эпидермальный ростовой фактор и IL-1 (а- и b-формы). Эти факторы действуют не только локально, вызывая костную резорбцию, но также могут в случае рака груди вызывать дальнейшее высвобождение РТНгР из опухолевых клеток.
Кроме прямого лизиса кости метастазами рак может вызывать гиперкальциемию удаленно, гуморальными механизмами — синдром гуморальной паранеопластической гиперкальциемии (ННМ). Синдром происходит в основном из-за циркуляции РТНгР, высвобождающегося из клеток опухоли, но другие цитокины тоже могут частично влиять, особенно при лимфоме и миеломе. Этот белок обладает близкой гомологией с РТН в первых 13 аминокислотах, но различается в остальных.
Скорее всего, альтернативные сплайс-варианты mRNA приводят к двум или более различным белкам. В большей части сквамозных карцином экспрессируется этот белок (есть у пациента гиперкальциемия или нет). С увеличением костной реабсорбции кальция его метаболические эффекты схожи с РТН.
Гиперкальциемия при раке может быть медицинским неотложным состоянием, особенно у пожилых и у пациентов с ми-еломой. Возросший уровень кальция в плазме может сопровождаться уремией, которая из-за потери воды и солей в результате действия кальция на дистальные почечные канальцы приводит к отсутствию реакции на антидиуретический гормон. Гиперкальциемию может также сопровождать гипокалиемия, развивающаяся частично из-за почечной потери калия.
У пожилых пациентов и пациентов с ухудшенной почечной функцией, не способных сопротивляться эффектам возросшей концентрации кальция в плазме, может быстро развиться угрожающая жизни почечная недостаточность. Такая ситуация особенно характерна при миеломе, поскольку присутствуют другие причины почечной недостаточности.
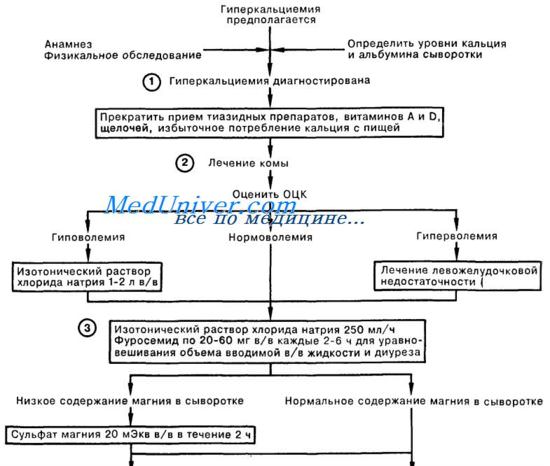
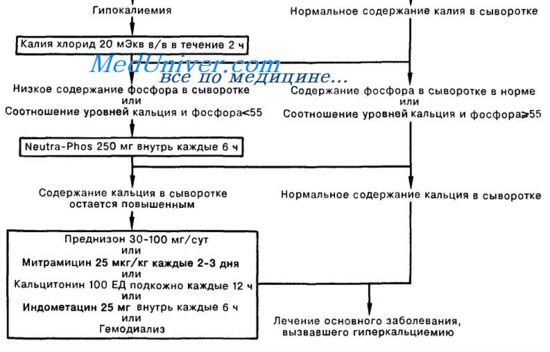
При серьезной гиперкациемии начальным лечением назначается замещение солей и воды с использованием изотонического раствора соли. В первые 24 ч потребуется 4—8 л. Этого бывает достаточно для снижения уровня кальция до нормального. За пожилыми пациентами надо внимательно следить, чтобы не перегрузить их жидкостями.
Если концентрация кальция в плазме не начинает спадать в течение 24 ч, дается перорально преднизолон (30-60 мг/день) или внутривенно гидрокортизон (50-100 мг каждые 6 ч), которые часто снижают кальций, но не у всех пациентов. Фруземид вызывает кальциурию, он должен приниматься осторожно с заменой объема во избежание дальнейшей потери воды и солей.
Бисфосфонаты уменьшают концентрацию кальция в сыворотке ингибированием костной резорбции и эффективны против гиперкальциемии, вызванной метастазами или PTHrp. Памидронат эффективен у 90% пациентов. Довольно часто его дают каждые два часа инфузионно в дозе 60-90 мг. Прием можно повторять каждые 2-3 недели. Бисфосфонаты вызывают жар и раздражение кожи, предпочтительно использовать их после регидратации, так как может произойти временное ухудшение работы почек.
Этидронат выглядит довольно менее эффективным — он обычно дается в виде трех вливаний по 7,5 мг/кг. Клодронат в дозе пяти вливаний по 300 мг ежедневно возвращает кальций к нормальному уровню в 90% случаев. Можно принимать клодронат перорально (1600 мг/день), но он вызывает желудочно-кишечные расстройства.
Митрамицин практически повсеместно был заменен бисфосфонатами. Обычная доза составляет 15-25 мг/день, разовая инфузия как правило вызывает падение кальция в плазме после 24-48 ч. Случается, что необходимо использовать митрамицин два или три последующих дня. Это приводит к риску развития тромбоцитопении.
Внутривенная или пероральная фосфатная терапия нечасто бывает необходима для контроля уровня кальция в плазме, но фосфатные вливания (обычно при уровне кальция в сыворотке 4 ммоль/л и больше) могут быть полезны для пациентов с камнями в почках.
Кальцитонин вызывает более быстрое падение уровня кальция в плазме, но его эффект непостоянный и использование ограничено пациентами с серьезной острой гиперкальциемией. Обычная доза составляет 2-4 МЕ/кг лососевого кальцитонина подкожно каждые 12 ч, или 1-2 МЕ/кг внутривенными вливаниями каждые 6 ч.
Хотя обычно не сложно установить диагноз того, что вызывает паранеопластическую гиперкальциемию, диагностические проблемы могут произойти, когда гиперпаратироидизм является альтернативным диагнозом у раковых больных, не обладающих признаками диссеминации рака.
Супрессивный тест с дексаметазоном не уменьшит уровня кальция в плазме при гиперпаратироидизме, но 75% раковых больных показывают его падение после 10 дней приема гидрокортизона. Если все еще имеются серьезные сомнения, следует помнить, повышение паратгормона в плазме найдено у 80% больных с первичным гиперпаратироидизмом, но не у пациентов с раком.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Кальциопенические состояния и их коррекция
Кальций (Са) — один из важнейших элементов в организме человека, особенности его метаболизма обусловливают физиологический гомеостаз и нормальное функционирование практически всех систем организма [1]. Наибольшее значение содержание и состояние метаболизм
Кальций (Са) — один из важнейших элементов в организме человека, особенности его метаболизма обусловливают физиологический гомеостаз и нормальное функционирование практически всех систем организма [1]. Наибольшее значение содержание и состояние метаболизма кальция имеет в детстве, пожилом возрасте, а также в период беременности [2].
Общие сведения о кальции. Кальций является самым распространенным элементом в теле человека, поэтому его относят к «макроэлементам». Организм взрослого в норме содержит примерно 25 000 ммоль (примерно 1000 г) кальция, из них 99% входят в состав скелета. Общее содержание минеральных веществ в человеческом организме — около 5% от массы тела, а на долю Са приходится почти треть от их общего количества [3].
По химическим свойствам Са относится к элементам, образующим прочные соединения с белками, фосфолипидами, органическими кислотами и другими веществами.
Функции Са. Кальций выполняет многочисленные функции в минеральном обмене, но этим его свойства не ограничиваются. Принято выделять следующие наиболее важные функции: участие в формировании и поддержании структуры костной ткани и зубов; активизация ферментных систем, обеспечивающих гемокоагуляцию и мышечное сокращение; участие в регуляции трансмембранного потенциала клетки, нервной и нервно-мышечной проводимости; поддержание сердечной деятельности; регуляция продукции и высвобождения гормонов и нейропептидов (нейромедиаторов); регуляция сосудистого тонуса; контроль всех этапов каскада свертывания крови; участие в важнейших метаболических процессах (гликогенолиз, глюконеогенез, липолиз и т. д.); функционирование в качестве «информационной» молекулы для многих ферментативных реакций; стимуляция секреторного и инкреторного процессов пищеварительных и эндокринных желез; pегуляция тонуса симпатической и парасимпатической нервной системы; биологическая сигнализация об активации всех стадий клеточного цикла и транскрипции генов; регуляция процессов внутриклеточного метаболизма; обеспечение стабильности клеточных мембран; препятствование высвобождению медиаторов аллергического воспаления; выполнение пластической роли при формировании тканевых и клеточных структур; способствование клеточной адгезии; участие в формировании кратковременной памяти и обучающих навыков; активация апоптоза и транскрипционного аппарата клеток (кофактор эндонуклеаз, участвующих в деградации ДНК при апоптозе); важна роль кальция в иммунологической активности (активация лимфоцитов, в частности, бластная трансформация в ответ на стимуляцию митогенами) [1, 2, 3].
Абсорбция кальция. Всасывается из верхних отделов тонкого кишечника, чему способствуют витамин D, аскорбиновая кислота, лактоза и кислая среда.
Всасыванию Са препятствуют избыток щавелевой кислоты, фитиновой кислоты, жиров, пищевых волокон и фосфатов. Один из важнейших механизмов поддержания уровня Са в крови — его экскреция с мочой, зависящая от фильтрации минерала и реабсорбции в почках [1].
Регуляция метаболизма кальция. Гипокальциемия, независимо от вызвавших ее причин, сопровождается снижением экскреции Са. Предполагается, что уменьшение выведения Са с мочой может происходить за счет увеличения накопления минералов в костной ткани или других тканях организма.
На регуляцию содержания Са в крови оказывают влияние: гормоны (в первую очередь, паратиреоидный гормон (ПТГ) и кальцитриол); сывороточные белки; содержание фосфатов (РО 3- 4) в сыворотке крови (реципрокные взаимоотношения).
Кальций депонируется в трабекулах костей; динамическое равновесие кальция поддерживается ПТГ и тиреокальцитонином. Pегуляция кальциевого гомеостаза является одной из наиболее сложных интегративных реакций организма человека, в осуществлении которой ведущая роль принадлежит нервной системе и железам внутренней секреции [1, 3].
Кальций и центральная нервная система (ЦНС). Гомеостаз Са имеет прямое отношение к ЦНС. Наряду с другими микро- и макроэлементами Са играет значительную роль в нейрофизиологических процессах. Еще в 1928 г. А. А. Богомолец подчеркивал исключительную важность Са в регуляции тонуса симпатической и парасимпатической нервной системы [1].
В нервной системе Са имеет значение в модуляции активности рецепторов к нейромедиаторам и нейропептидам. Повышенное высвобождение Ca способствует ишемическому повреждению нейронов вследствие вазоконстрикции и инициации каскада апоптоза [1, 3, 4]. Конкурентные взаимоотношения между различными микроэлементами (Zn, Hg, Cu, Cd) и кальцием могут определять самые разнообразные биологические эффекты и, в конечном счете, — течение неврологических процессов [4].
При рассмотрении Са на клеточном уровне необходимо выделять его участие в регуляции ионной проницаемости мембраны нейрона, генерации возбуждения.
При гипокальциемии различного генеза могут отмечаться симптомы, имеющие отношение к сфере неврологии: отклонения в поведении; онеменение и парестезии; судороги; спазмы мышц; положительные симптомы Хвостека или Труссо (гипопаратиреоз) и т. д. Нарушениям обмена Са нередко сопутствуют фебрильные судороги, пароксизмы гипоксического, метаболического или эндокринного генеза, нейрофиброматоз (1-го типа), гидроцефалия, краниостеноз и ряд других видов патологии ЦНС [1, 4]. У детей первых лет жизни ярким примером кальциопенической соматоневрологической патологии является классический (витамин D-дефицитный) рахит [2].
Существуют данные, свидетельствующие о том, что действие Са зависит от типа нервной деятельности и ее функционального состояния. На необходимость коррекции нарушений содержания Са в организме детей грудного и раннего возраста при неврологических заболеваниях указывает Е. М. Мазурина (2005) [2].
Следует помнить, что избыточное накопление в организме Са может привести к нейротоксичности, угрозе патологической кальцификации стенок сосудов и тканей организма [3, 4].
Потребность в кальции. Ha первом году жизни она составляет (по разным данным) от 350 мг до 1000 мг/сут, на втором — 370–1000 мг/сут, на третьем — 300–1000 мг/сут. У детей более старшего возраста и взрослых она возрастает до 1000–1500 мг/сут [1, 2]. Внимания заслуживает то обстоятельство, что в разных странах мира рекомендации по суточной потребности в Са2+ значительно отличаются. По-видимому, это объясняется особенностями разных регионов (климато-географическими, экологическими и др.).
Алиментарное поступление Са имеет огромное значение в любом возрасте. J. C. Leblanc et al. (2005) изучены паттерны диетического потребления 18 элементов во Франции, a R. B. Ervin et al. (2004) — отдельных минеральных веществ в США [5, 6]. Применительно к Са они признаны неудовлетоворительными в обеих странах.
Нормы содержания кальция в организме. Считается, что около 70% Са экскретируется с калом, 10% — c мочой, а ретенция элемента составляет 15–25% (в зависимости от темпов роста).
Сывороточное содержание Са (в норме) равняется 9–11 мг%, причем 50–60% — в ионизированной форме. У здоровых детей независимо от возраста в сыворотке крови содержится 4,9–5,5 мг% (1,22–1,37 ммоль/л) ионизированного Ca, исходя их данных, полученных с использованием ион-селективных электродов. Экскреция Са с калом (при следовании обычной диете) составляет менее 140 ммоль/сутки (560 мг/сутки). Определяется прямая зависимость содержания Са в кале от особенностей диеты.
Содержание Са в моче также находится в прямой зависимости от количества алиментарно потребляемого элемента. В частности, при нормальной диете суточная экскреция равняется 2,5–7,5 ммоль/сут (100–300 мг/сут, 5–15 мЭкв/сут). При потреблении Са на уровне менее 200 мг/сут — 0,33–4,5 ммоль/сут (13–180 мг/сут), 200–600 мг/сут — 1,25–5,0 ммоль/сут (50–200 мг/сут), 1000 мг/сут — 7,5 ммоль/сут (до 300 мг/сут) [1, 2].
Снижение содержания кальция в физиологических средах организма. Наиболее значимо снижение Са в сыворотке крови. В этой физиологической жидкости Са представлен тремя следующими формами: связанный с белками (недиффундирующий — 30–55%); хелатированный (диффундирующий, но неионизированный — около 15%); ионизированный Са (около 30–55%) [3].
Физиологическое снижение содержания Са в крови может отмечаться при повышенной утилизации углеводов или назначении инсулина. Патологическое снижение содержания Са свойственно следующим клиническим ситуациям: гипопаратиреоидизм (следствие хирургического вмешательства в области паращитовидных желез); псевдогипопаратиреоидизм; дефицит витамина D; стеаторея (сочетанные нарушения абсорбции витамина D, Ca и РО 3- 4); нефрит (снижение неионизированной фракции Са, переносимой белками сыворотки, по-видимому вследствие потери Са с мочой); болезни почек с ретенцией фосфатов; острый панкреатит; внутривенное введение солей Mg, оксалатов или цитратов; остеопороз у пожилых людей (нижняя граница нормы); неонатальная гипокальциемия (первый день жизни — вследствие низкой массы тела при рождении, острой интранатальной асфиксии, наличия у матери сахарного диабета, гиперпаратиреоза или нелеченой целиакии; недоразвития плаценты, гестоза, оперативных родов посредством кесарева сечения, при заменных переливаниях крови; 5–10 день — вследствие гиперфосфатемии, вызванной потреблением коровьего молока или малоадаптированных смесей на его основе); гипомагниемия; длительный прием антиконвульсантов (обычно при эпилепсии); состояние после удаления щитовидной железы; болезнь Педжета — при лечении кальцитонином. Особое внимание в отечественной и зарубежной литературе различных лет уделяется кальциопеническим состояниям при остеопорозе и сходных с ним видах костной патологии [1].
Снижение содержания Са в кале обнаруживается в следующих случаях: остеомаляция, успешно вылеченная препаратами витамина D; гипервитаминоз D; низкое содержание фосфора в рационе питания; саркоидоз Бека (в некоторых случаях).
В моче снижение содержания Са возможно при низком потреблении этого макроэлемента с пищей, а кроме того, нередко отмечается на поздних сроках беременности.
Концентрация Са в спинномозговой жидкости (СМЖ) составляет около 1/2 от сывороточного содержания. Изменения в содержании Са в СМЖ невелики, а их регистрация не имеет большого значения для диагностики различных патологических состояний. Уровень Са в СМЖ может снижаться у некоторых пациентов с эпилепсией, длительно получающих терапию фенитоином и другими аниэпилептическими препаратами (АЭП). Практически все известные к настоящему времени АЭП обладают Са-изгоняющими свойствами. Дети грудного и раннего возраста, страдающие эпилепсией, наиболее подвержены риску гипокальциемии [1].
Методы коррекции кальциопенических состояний. Если при острых нарушениях концентрации Са в сыворотке крови тактика лечения уже давно разработана и является почти хрестоматийной, то в области профилактики и коррекции умеренной гипокальциемии до сих пор отмечается определенный пробел.
В различных областях медицины нередко имеет место эмпирический подход к данной проблеме. Попытки компенсировать индуцированный приемом антиконвульсантов дефицит Са за счет приема антиэпилептических препаратов, в состав которых включены соли кальция, в подавляющем большинстве случаев малоэффективны. Так, одна 300-миллиграммовая таблетка препарата Конвульсофин содержит всего 33 мг кальциевой соли, а в составе Паглюферала обнаруживается 250 мг глюконата Са (в составе глюферала — 200 мг). Указанные количества макроэлемента явно недостаточны для нивелирования Са-изгоняющих эффектов этих антиэпилептических средств.
Широкая распространенность, мультифакториальность и потенциальная предотвратимость кальциопенических состояний предполагают необходимость совершенствования методов их профилактики и коррекции. J.-Y. Reginster et al. (2002) подчеркивает влияние ежедневного приема Са и витамина D на секрецию гормонов паращитовидной железой [7]. Сомнения относительно существующих рекомендаций по профилактическому приему препаратов Са и витамина D высказывали A. Prentice (2002) и J. A. Amorim Cruz (2003) [8, 9]. H. L. Newmark et al. (2004) считают необходимым добавление Са и кальциферола в зерновые продукты промышленного производства [10]. В отличие от профилактики кальциопенических состояний, в их коррекции диета малоэффективна. Поэтому для коррекции дефицита Са в организме используются препараты, содержащие этот макроэлемент [1, 2].
Препараты кальция, используемые в медицине, и показания к их применению. В используемых справочниках лекарственных средств приводятся следующие основные формы кальция: хлорид, глюконат, лактат, карбонат и цитрат, хотя данный макроэлемент может быть представлен и другими соединениями (кальция фолинат, ацетат, g-гидроксибутират, глицерофосфат, глутаминат, добезилат, пангамат, пантотенат, тринатрия пентенат, фосфат и др.) [11, 12, 13].
В числе показаний к назначению основных перечисленных препаратов Са фигурируют следующие: недостаточная функция паращитовидных желез, сопровождающаяся тетанией или спазмофилией; усиленное выделение Са из организма (при длительной обездвиженности больных, синдромах мальабсорбции или приеме АЭП); аллергические заболевания; уменьшение проницаемости сосудов; кожные заболевания; паренхиматозный гепатит; токсические поражения печени; нефрит; гиперкалиемическая форма пароксизмальной миоплегии; хроническая почечная недостаточность; остеопороз [11, 12, 13].
В литературе последних лет представлены и другие показания к применению препаратов Са: синдром хронической усталости; сахарный диабет; артериальная гипертензия у детей с солевой чувствительностью. Помимо этого, кальций может назначаться для повышения свертываемости крови (как гемостатическое средство). В качестве показаний к использованию препаратов Са необходимо привести различные виды рахита (витамин D-зависимый, витамин D-резистентный, витамин D-дефицитный, остеопения маловесных детей и т. д.) [1].
К сожалению, даже при продолжительном назначении препаратов, обладающих Са-изгоняющим действием, а также других лекарственных средств, индуцирующих гипокальциемию, рутинной коррекции уровня кальция обычно не проводится, а в существующих рекомендациях подобной процедуры не предусмотрено.
Положительный эффект препаратов кальция проявляется только при индивидуальном подборе их дозировки. При назначении всегда необходимо учитывать утилизацию (усвоение) данного макроэлемента, выраженную в процентах от назначаемого количества. В частности, для глюконата, лактата и хлорида кальция она составляет соответственно 9%, 13% и 27%. Для карбоната и цитрата кальция характерны более высокие показатели всасывания из кишечника. B. W. Downs et al. (2005) cообщают о высокой биологической эффективности новой соли на основе кальций-калиевого соединения гидроксицитрусовой кислоты [14].
Литература
В. М. Студеникин, доктор медицинских наук, профессор
Э. М. Курбайтаева
НЦЗД РАМН, Москва
Лечение бисфосфонатами гиперкальциемии
при раке молочной железы
Паранеопластическая гиперкальциемия – не такое уж редкое явление, частота ее при некоторых заболеваниях достигает 10-15%. Обычно она выявляется на поздней стадии опухоли, но иногда бывает первым симптомом заболевания. Это касается, как правило, гуморальной гиперкальциемии – одного из вариантов опухолевой, развивающейся вследствие секреции опухолью веществ – ПТГ-подобных пептидов, стимулирующих костную резорбцию. В качестве примера можно привести гуморальную гиперкальциемию при плоскоклеточном раке легкого или гипернефроме, когда для развития патологического состояния наличие метастазов в кости совсем не обязательно. Выделяемые опухолью вещества меняют метаболизм костной ткани, усиливая активность остебластов и остеокластов. Второй вариант паранеопластической гиперкальциемии – остеолитическая, возникающая вследствие разрушения опухолью костной ткани. При раке молочной железы гиперкальциемия имеет признаки обоих вариантов. Превалирует вариант остеолитической гиперкальциемии, когда опухолевые клетки не только сами разрушают кость, но и выделяют цитокины, простагландины группы Е, активирующие остеокласты и стимулирующие резорбцию кости вблизи метастазов. Клетки рака молочной железы также секретируют паратгормонподобные пептиды, что является признаком гуморальной гиперкальциемии.
Особая форма гиперкальцемии, так называемая «tumor flare hypercalcemia», возникает у 5-6% больных раком молочной железы в первые 6 недель приема тамоксифена или прогестинов. Такую индуцированную лекарством гиперкальциемию весьма успешно лечат бисфосфонатами без отмены эндокринных препаратов [44].
Гиперкальциемия может быть связана с передозировкой препаратов витамина D. Дефицит витамина D возникает при нарушении его всасывания при ряде неопухолевых заболеваний, недостаточной инсоляции с октября по март. Не секрет, что под действием рекламы многие больные раком молочной железы принимают препараты витамина D без каких-либо оснований. Такую гиперкальциемию лечат отменой препарата, бисфосфонаты здесь неуместны.
Симптомы гиперкальциемии появляются при кальции выше 3 ммоль/л, но это совсем не обязательно – между степенью гиперкальциемии и клиническими проявлениями нет четкой зависимости. Иногда высокий кальций крови бывает случайной находкой. Паранеопластическая гиперкальциемия может проявляться утомляемостью, депрессией, спутанностью сознания, отсутствием аппетита, тошнотой, рвотой, обратимым нарушением функции почечных канальцев, аритмией. Поэтому при подозрении на гиперкальциемию необходимо сразу же сделать анализ крови на кальций. Отсрочив это исследование и отправив пациентку домой на 1-2 суток, вы рискуете потерять ее. Тяжелая гиперкальциемия с уровнем кальция свыше 3,7 ммоль/л опасна развитием комы и остановкой сердца. Под маской удовлетворительного самочувствия при симптомах минимальной выраженности может скрываться отнюдь нелегкая гипекальциемия.
К большому сожалению, зная о клинических проявлениях гиперкальциемии и градации тяжести по содержанию кальция крови, мы забываем о том, что при патологических состояниях не следует брать за основу уровень общего кальция крови, состоящий из трех фракций: 40% его связано с белками, 10% – сверхионизированные ионы и половина – ионизированный. В организме здорового человека содержится 1-2 кг кальция, из них 98% – в составе костной ткани. Лишь 0,5% общего кальция кости свободно обменивается с кальцием внеклеточной жидкости. Постоянное изменение кальция связано с PH плазмы и состоянием кишечника и почек, контролируется минимум тремя гормонами. Только ионизированный кальций является величиной постоянной и меняется при болезнях костной ткани [4].
Норма сывороточного (общего) кальция 8,5-10,3 мг% или 4,2-5,2 мэкв/л или 2,2-2,6 ммоль/л; ионизированного – 4,2-5,2 мг% или 2,1-2,б мэкв/л или в среднем 1,2 ммоль/л; в системе СИ: общий 2,1-2,2 ммоль/л, ионизированный 1,05-1,3 ммоль/л [1]. При невозможности прямого измерения соотношение ионизированного и связанного кальция можно оценить по формуле [40]:
Связанный с белком кальций (%) = 0,8×Альбумин (г/л) + 0,2×Глобулин (г/л) + 3
В своем уже ставшим классическим постоянно обновляемом труде «Bisphosphonates in Bone Disease» Herbert Fleisch, проанализировав огромное количество литературы, делает вывод, что для лечения острой гиперкальцемии сложно отдать предпочтение какому-либо препарату – клодронату, памидронату или ибандронату, а при хронической гипер-кальцемии клодронат оральный и внутривенный памидронат одинаково эффективны [14].
Еще в 1994 г. Green J.R с соавторами показали, что активность незначительно различалась между клодронатом и паминдронатом, значительно повышалась in vitro на клетках мышей, in vivo на крысах эти различия усугублялись [15]. Проспективное исследование, проведенное с включением 8905 здоровых женщин с различной минеральной плотностью кости, показало, что вероятность развития метастазов в кости выше, чем выше минеральная плотность кости, тогда как при остеопорозе этот показатель ниже [39]. Казалось бы, что лизис кости при остеопорозе должен быть более благоприятен для возникновения на этом фоне метастазов, но получается как раз наоборот. И если у одного биологического типа, при кажущейся сходности механизма патологической резорбции и формирования кости, отмечаются такие различия, то при сравнении терапевтического эффекта лекарственного препарата у различных биологических типов эти различия многократно увеличиваются. Вот почему нельзя считать, что ибандронат у женщин будет эффективнее памидроната в 10-100 раз, а клодроната в 100-1000. В отличие от крыс сила ингибирования бисфосфонатами костной резорбции у человека в десятки раз ниже.
Рандомизированное исследование сравнительной эффективности рекомендованных доз ибандроната и памидроната при гиперкальциемии, проведенное в 19 центрах на 72 больных, стратифицированных по уровню исходного кальция и ежедневным мониторингом, дало следующие результаты. Среднее снижение исходного уровня кальция через 4 дня в группе ибандроната было выше, чем для всей когорты, получившей памидронат. Частота эффекта, продолжительность и время начала снижения кальция были одинаковы для обеих групп. Однако у 11 больных с исходным уровнем кальция 3,4-4,0 ммоль/л среднее снижение в группе ибандроната было выше в два с лишним раза, чем при использовании памидроната. Таким образом, преимущество ибандроната при опухоль-ассоциированной гиперкальциемии выявляется при исходном уровне кальция не ниже 3,5 ммоль/л. Следует отнести к преимуществам и возможность более быстрого введения ибандроната (30-минутная инфузия на 250 мл физиологического раствора), что не увеличивает по сравнению с 2-часовой процент негативных реакций [25].
В архивных данных фирмы Хоффманн-Ля Рош есть подтверждение того, что ибандронат более эффективен при остеолитической гиперкальциемии, чем гуморальной. При дозе препарата 2 мг эффект регистрировался у 63% и 57% соответственно. Ибандронат в дозе 4 мг был результативен у 84% против 68% при гуморальном варианте. При раке молочной железы могут быть оба варианта, но чаще – остеолитический [63].
На протяжении 20 лет роль клодроната для лечения опухоль-ассоциированной гиперкальциемии подробно изучалась. В большинстве работ показана высокая эффективность – до 90% [30]. Возможно использование как 5-дневных инфузий, так и однократное введение 1500 мг препарата [45], но не в тех ситуациях, когда требуется действительно скорая помощь, то есть при тяжелой гиперкальциемии. Найдется очень мало врачей, рискнувших ввести одномоментно пятидневную дозу препарата в 1500 мг, – не из-за боязни токсических реакций, а из-за перспективы последующего разбирательства с администрацией учреждения, приверженной традиционным подходам. Поэтому лучше клодронат применять при легкой или средней степени гиперкальциемии, «мягко» снижая кальций на протяжении 5 суток.
Золедронат, по сравнению с памидронатом, эффективнее нормализовал концентрацию кальция в сыворотке: 32% дня против 18% [22]. Эффект золедроната в два раза продолжительнее. Импонирует и несомненная простота инфузии зометы. Но это не сулит экономии, поскольку стоимость зометы значительно выше аредии.
Думаю, следует согласиться с доктором Fleisch и на практике использовать для лечения гиперкальциемии любой из 4 препаратов. Ограничения на лечение накладываются только спектром токсических реакций, о которых будет сказано ниже.
В амбулаторной практике нечасто регистрируется тяжелая гиперкальциемия, таких больных необходимо госпитализировать из-за возможности развития комы. Ведь лечение гиперкальциемии не может ограничиться только введением бисфосфонатов, необходимо восстановить ОЦК, форсировать диурез и при этом восполнить потери натрия. Легкую гиперкальциемию вполне можно купировать и в амбулаторных условиях, надо только быть уверенным, что это действительно легкая степень.
Согласен Данный веб-сайт содержит информацию для специалистов в области медицины. В соответствии с действующим законодательством доступ к такой информации может быть предоставлен только медицинским и фармацевтическим работникам. Нажимая «Согласен», вы подтверждаете, что являетесь медицинским или фармацевтическим работником и берете на себя ответственность за последствия, вызванные возможным нарушением указанного ограничения. Информация на данном сайте не должна использоваться пациентами для самостоятельной диагностики и лечения и не может быть заменой очной консультации врача.
Сайт использует файлы cookies для более комфортной работы пользователя. Продолжая просмотр страниц сайта, вы соглашаетесь с использованием файлов cookies, а также с обработкой ваших персональных данных в соответствии с Политикой конфиденциальности.