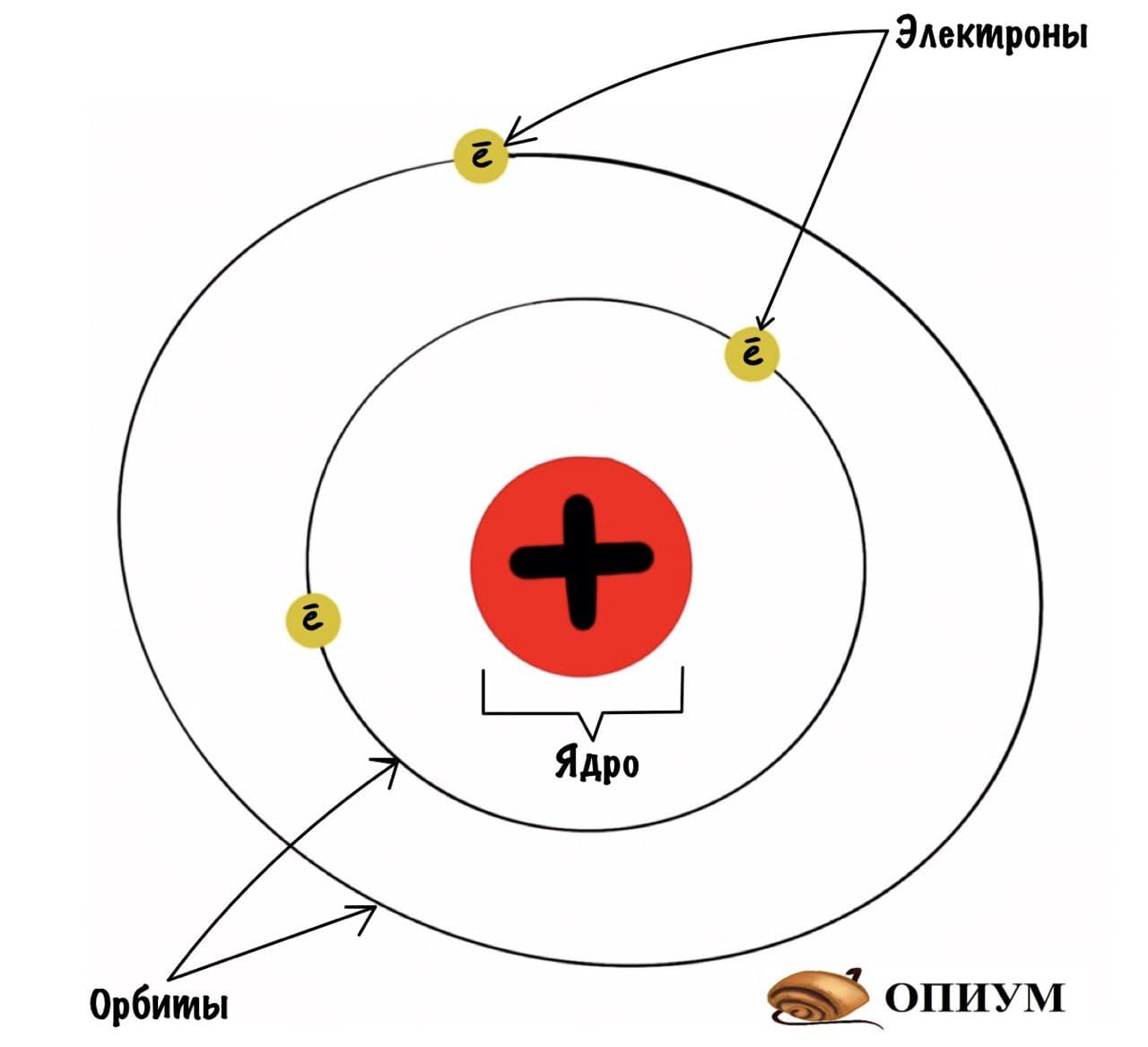
Как называется современная модель атома
Современная модель строения атома



В основе современной теории строения атома лежат работы Дж. Томсона (который в 1897 г. открыл электрон, а в 1904 г. предложил модель строения атома, согласно которой атом – это заряженная сфера с вкрапленными электронами (модель «кекс с изюмом»)), Э. Резерфорда (который в 1910 г. открыл ядро и предложил ядерную планетарную модель атома), М. Планка (который в 1900 г. высказал предложение, что вещества поглощают и пропускают энергию дискретными пропорциями, названными им квантами), Н. Бора (который в 1910 г. предложил модель строения атома водорода), А. Эйнштейна (который в 1905 г предсказал, что любое излучение представляет собой поток квантов энергии, назваными им фотонами), Луи де Брайля (который в 1924 г. выдвинул предложение, что электрон характеризуется также корпускулярно-волновым дуализмом), В. Гейзенберга (который в 1927 г. постулировал принцип неопределенности), Э. Шредингера (который в 1926 г. вывел математическое описание поведения электрона в атоме) и многих других. Работы этих ученых заложили основу квантовой механики, изучающей движение и взаимодействие микрочастиц.
Современная модель строения атома базируется на четырех положениях:
2. Положительный заряд и почти вся масса атома сосредоточены в ядре атома.
3. Ядра атомов состоят из протонов и нейтронов (общее название нуклоны). Число протонов в ядре равно порядковому номеру элемента, а сумма чисел протонов (p) и нейтронов (n) соответствует его массовому числу.
4. Вокруг ядра по орбиталям вращаются электроны. Число электронов в невозбужденном (основном) сост. равно заряду ядра (табл. 1).
Различные виды атомов имеют общее название – нуклиды. Нуклиды с одинаковым зарядом, различными массовыми числами и числом нейтронов в ядре называется изотопами. Нуклиды с одинаковыми массовыми числами, но различными зарядами ядра и числа нейтронов в ядре называются изобарами. Нуклиды с одинаковым числом нейтронов, но различным зарядом и массовым числом называется изотонами.
В соответствии с представлениями квантовой механики, электрон обладает двойственной природой, т.е. корпускулярно-волновым дуализмом: с одной стороны электрон – это частица, которая имеет массу, заряд и скорость движения; а с другой стороны электрон проявляет волновые свойства, такие как способность к дифракции, интерференции и особенности движения. Согласно принципу неопределенности В. Гейзенберга невозможно точно определить энергию и положение электрона, поэтому в квантовомеханической модели атома используют вероятностный подход для характеристики положения электрона. Вероятность нахождения электрона в определенной области пространства описывается квадратом волновой функции Ψ 2 (пси), которая характеризует амплитуду волны, как функцию координат электрона. Электрон может находиться в любой части околоядерного пространства, однако вероятность его нахождения в разных частях этого пространства неодинакова.
Свойства электронных частиц образующих атомы
Пространство вокруг ядра, в котором вероятность нахождения электрона достаточно велика, называется орбиталью.
Орбиталь характеризует вероятность нахождения электрона в определенном пространстве вокруг ядра. Она ограничена в трехмерном пространстве поверхностями той или иной формы. Вероятность нахождения электрона внутри данной области пространства составляет не менее 95 %.
Современная модель атома: характеристики, постулаты и влиятельные ученые
Содержание:
Это наиболее широко принятая и используемая модель при изучении структуры атомов, молекул и химической реакционной способности элементов благодаря точности ее предсказаний и относительной простоте.
Эта модель является развитием нескольких предыдущих атомных моделей, таких как модель Резерфорда и модель Бора-Зоммерфельда, которые считались классическими или полуклассическими моделями.
В настоящее время существуют теоретически более полные модели, чем квантово-механическая модель Шредингера, например модель Дирака-Жордана, которая включает специальную теорию относительности и основана на волновом уравнении Дирака. В этом уравнении спин, свойство электронов, упомянутое в начале, проявляется естественным образом.
Существуют также модели, основанные на квантовой теории поля, применяемые в физике высоких энергий. Эти модели отлично подходят для предсказания создания и уничтожения элементарных частиц, что является целью этой области физики.
Следует отметить, что наиболее сложные теории сходятся к тем же результатам, что и уравнения Шредингера, особенно для легких атомов.
Характеристики современной атомной модели
В нынешний взгляд на атом, основанный на нерелятивистской квантовой механике, концепция электронных орбит в стиле планетных систем не подходит.
Однако наиболее распространенным изображением атома по-прежнему остается изображение положительного центрального ядра и нескольких точек отрицательного электрического заряда (электронов), вращающихся по идеально определенным орбитам вокруг центрального ядра. Но, несмотря на свои корни, он больше не соответствует нынешней атомной модели.
На рисунке 2 показаны старое и текущее изображения атома гелия в его низком энергетическом состоянии (уровень n = 1 и l = 0).
Классическое изображение полезно для того, чтобы увидеть, что ядро содержит два протона и два нейтрона. Гарантируя нейтральность атома, два электрона занимают один и тот же энергетический уровень.
Классическая механика утверждает, что каждая материальная частица имеет связанную волну, называемуюволновая функция. Это знаменитый волновая дуальность Луи де Бройля.
В современной атомной модели поведение электрона в масштабе атомов заметно волнообразно, тогда как на макроскопическом уровне, как электроны, движущиеся в электронно-лучевых трубках старых телевизоров, преобладает корпускулярное поведение.
С другой стороны, с фотонами происходит обратное: в большинстве оптических явлений (на макроскопическом уровне) они имеют принципиально волновое поведение. И когда они взаимодействуют с атомами материи, они имеют поведение частиц.
Из-за этого электроны вокруг ядра рассеиваются в областях, называемых атомные орбитали, форма и протяженность которого будут зависеть от уровня энергии электронов и углового момента.
И энергия, и угловой момент электрона вокруг ядра имеют определенные допустимые значения, поэтому они называются квантованный.
Волновое уравнение Шредингера предсказывает допустимые значения энергии и углового момента, а также волновую функцию, связанную с каждым уровнем энергии и импульсом.
Математический квадрат волновой функции определяет орбитали, то есть области вокруг ядра, где электроны с наибольшей вероятностью встретятся.
Размер атома
Чтобы получить масштабное изображение текущей модели атома, давайте представим, что диаметр атома равен диаметру футбольного поля. Ядро было бы похоже на муравья в центре поля, но удивительно 99,9% атомной массы.
С другой стороны, электроны будут похожи на призрачных игроков, разбросанных по полю, с большей вероятностью их можно найти в центре поля.
Есть несколько допустимых выравниваний или способов занять поле, которые зависят от энергии игроков (электронов) и количества «вращения» или вращения вокруг центра.
Постулаты современной атомной модели
1.- Электрон характеризуется своей массой m, своим спином s и потому что это частица, несущая элементарный отрицательный заряд (-e).
2.- Электроны имеют двойное поведение, одновременную волну-частицу, но в зависимости от их энергии и масштаба явления одно может быть более распространенным, чем другое.
3.- Электроны окружают положительное атомное ядро таким образом, что они гарантируют электрическую нейтральность атома. Следовательно, количество электронов равно количеству протонов; Это атомный номер, который дает химические и физические характеристики каждого элемента.
4.- Взаимодействие между электронами и ядром моделируется потенциалом V (р) электростатический кулоновский, к которому член потенциальной энергии включен в гамильтонов оператор.
7.- При поиске стационарных решений электронной волновой функции используется не зависящее от времени уравнение Шредингера:
H Ψ (р) = E Ψ (р)
Где E представляет собой полную энергию электрона.
8.- В атомах с несколькими электронами взаимодействие между ними не учитывается.
9.- Когда дело доходит до атомов, состоящих из многих электронов, орбитали крайних электронов моделируются потенциалом ядра, экранированным самыми внутренними электронами, который известен как потенциал Дебая.
10.- Уравнение (7) имеет решение для некоторых дискретных значений энергии, так что знаменитый планковские кванты, естественно возникают из решений уравнения Шредингера.
11.- Для каждого дискретного значения E существует волновая функция. Но некоторые решения вырождены в зависимости от значения углового момента L.
14.- Спин не появляется в уравнении Шредингера, но он включен в атомную модель через принцип Паули:
Таким образом, одно и то же состояние, характеризуемое квантовыми числами n, l, m уравнения Шредингера, может быть занято не более чем двумя электронами с противоположными спинами. Таким образом, спин становится четвертым квантовым числом.
Влиятельные ученые в современной модели атома
Это кажется невероятным, но большинство физиков, внесших вклад в текущую модель атома, изображены на одной фотографии. Они познакомились на знаменитых конференциях, организованных Эрнестом Солвеем, химиком и промышленником бельгийского происхождения, прославившимся в мире науки.
Они начали проводиться в 1911 году и собирали крупнейших ученых того времени, среди которых были практически все, кто внес свой вклад в нынешнюю атомную модель.
Самая известная из этих конференций состоялась в Брюсселе в 1927 году, и здесь была сделана эта историческая фотография:
Строение атома
История открытия. Демокрит. Начала атомистики
Уже в древности философы задумывались, из чего же состоит природа вокруг них. Демокрит первым из античных ученых предположил, что все в мире состоит из крошечных неделимых частиц. Эту частицу он назвал атом, что в переводе с греческого означает «неделимый».
К сожалению, возможности ученых в те времена были весьма ограничены. Каких-либо приборов, позволяющих исследовать строение вещества, у них не было. Но значение Демокрита в зарождении атомистики невозможно сбросить со счетов истории.
Атомно-молекулярное учение. Строение атома
Практически до середины XVIII века, пока М.В. Ломоносов не принес в химию количественные эксперименты, учение об атомах оставалось лишь прерогативой философских размышлений. Михаил Васильевич считал, что лишь знание физических законов поможет правильно истолковать результаты химических опытов.
В своих исследованиях ученый выделил в веществе крупные частицы — «корпускулы», и мелкие — «элементы», или как мы называем их сейчас — атомы.
Ломоносов считал, что каждая молекула по своему составу идентична всему веществу, а также, что различные по химическому строению элементы имеют и разные по составу молекулы. Ученый предполагал, что вещества имеют особенности не только из-за отличий в составе молекул, но и благодаря различному расположению атомов в молекуле.
Следующий шаг в изучении атомов сделал английский естествоиспытатель Джон Дальтон. Проводя различные эксперименты с растворением газов в жидкостях, ученый открыл главное физическое качество атомов: эти мельчайшие частицы имеют вес. Но поскольку атом до сих пор никто не видел, Дальтон назвал вес частицы относительным. Он установил, что самым легким элементом является водород и предложил его вес принять за единицу.
Открытие Дальтона стало прорывом в химии. Ведь теперь к любому химическому соединению можно было подойти с измерительным прибором. Это исследование позволило приблизиться к современной записи химических формул и уравнений. И именно Дальтон придумал первые обозначения для известных химических элементов.
До конца XIX века, несмотря на все старания ученых, химическое строение атома по-прежнему оставалось лишь гипотезой.Ученым не хватало оборудования, чтобы постичь тайну мельчайшей частицы.
Открытие Дальтона дало толчок дальнейшим опытам, в ходе которых ученые вычислили относительную атомную массу разнообразных химических элементов, что позволило их классифицировать, а Д.И.Менделееву – сформулировать периодический закон и представить научному миру Периодическую систему химических элементов.
Протоны и нейтроны
Обнаружение катодных лучей немецким ученым-физиком Юлиусом Плюккером в 1859 году и создание прототипа электронной трубки Ульямом Круксом в 1879 году положили новый виток исследованиям в атомистике.
Однако потребовалось еще несколько десятков лет, чтобы строение атомов химических элементов приоткрыло свои тайны. на заре XX века в одном журнале появились две публикации, которые пытались объяснить структуру атома. Одна из публикаций принадлежала английскому ученому Д.Д. Томсону, автором другой был японский физик Хантаро Нагаока.
При создании своей атомной структуры Нагаока использовал разработанную Максвеллом в 1856 году теорию устойчивости колец Сатурна. Японский ученый был убежден, что опираясь на «сатурнианскую» модель ядра в будущих исследованиях, можно прояснить все основные свойства материи.
Исследователь ошибся, однако два постулата его теории впоследствии подтвердились:
Томсон выдвинул гипотезу о том, что атом напоминает шарообразную, электронейтральную сферу диаметром около 10 –10 м, где положительный заряд равномерно распределен по всей структуре атома, а электроны хаотично расположены в этом поле. Поэтому, можно сказать, что атом напоминает микроскопическую булочку с изюмом.
Опыты продолжались в разных странах. В лаборатории Резерфорда проходили испытания, которые смогли доказать, что в центре атома расположено крупное ядро с диаметром около —10 —15 м, в котором содержится более 99,95 % его массы, а заряд его положительный.
В 1932 году и Джеймс Чедвик обнаружил нейтрон — третий недостающий элемент атома.
Атомное взаимодействие обеспечивает тесную связь протонам и нейтронам в ядре атома. Протоны и нейтроны имеют общее название — нуклоны. Ученые считают, что их характеристики достаточно подобны, чтобы отнести эти частицы к одному семейству, как биологи относят в один вид собак и волков.
Казалось бы, вот оно – тайна ядра разгадана. Но нет, в современной физике считается, что нуклоны состоят из еще более мелких частиц, которые называют кварками, и кварковая модель является ведущей в современной науке.
Эксперименты по исследованию атома и его ядра не прекращаются, и в 2010 году международная группа физиков при исследовании протонов в мюонном водороде установила, что размер радиуса протона меньше на 4%, чем считалось до этого.
Так в фундаментальную физику ворвалась загадка протонного радиуса, почему измерение одной и той же величины в обычном и в мюонном водороде дает разные результаты — и, несмотря на усилия сотен специалистов, она до сих пор не решена.
Изотопы
Работая в лаборатории Резерфорда, Фредерик Содди экспериментально установил, что встречаются атомы одного химического элемента с различной атомной массой. А поскольку к этому времени уже было известно, что количество протонов для ядра постоянно, соответственно, отличались они количеством нейтронов.
Содди предложил термин изотоп (от греческих слов изос — «равный» и топос — «место») для обозначения веществ, идентичных по химическим свойствам, но отличающихся атомной массой и определенными физическими свойствами.
При графической записи изотоп выглядит как знак химического элемента, которому он соответствует. А что бы обозначить разницу, в массовом числе используют индекс слева вверху: ( 12 C, 222 Rn)
Протий, дейтерий, и тритий — исторические собственные названия изотопов водорода.
Электронное строение атома
Исследование таинственного микромира продолжается. Изучение движения электронов и внутриатомных взаимодействий выделилось в отдельную область физики — квантовую механику. Главный постулат квантовой механики — все волны обладают свойствами частиц, а микрочастицы имеют волновую природу.
В макромире физическое тело всегда находится в какой-то конкретной точке пространства. Даже если вы сфотографируете летящую муху и на фотографии она будет в виде черной полосы, вы все равно будете уверены, что в конкретный момент времени она была в определенном месте.
В мире атома все иначе. Легкий подвижный электрон находится одновременно во всех точках околоядерного пространства. Если провести аналогию с макромиром, больше всего это напомнит неплотный клубок мягкой пушистой шерсти.
И именно эта зона пространства, где существует вероятность встретить электрон, называется электронным облаком. Плотность электронного облака неравномерна.
В электронном облаке выделяют зону, где вероятность встречи с электроном более 90% — эта область обозначена как атомная или электронная орбиталь.
Все электроны в атоме обладают определенной энергией. Чтобы описать состояние электрона, ученые используют квантовые числа. Всего их четыре. Целое число n, которое определяет энергию электронов на конкретном энергетическом уровне, называют главным квантовым числом.
На одной электронной оболочке находятся атомные орбитали с единым значением главного квантового числа n.
У невозбужденного атома электроны расположены на орбиталях 4-х видов: s, p, d и f.
Но почему нельзя было обозначить буквами по алфавиту a, b, c? Все не так просто, для обозначения атомных орбиталей ученые решили использовать начальные буквы от прилагательных, описывающих спектральные линии в атомных спектрах:
Чтобы графически представить расположение электронов на уровнях и подуровнях атомной оболочки, ученые ввели электронные формулы. Это такие численно-буквенные комбинации, где подуровень обозначен строчной латинской литерой, а цифровой индекс вверху справа обозначает количество электронов на подуровне.
Несмотря на свои способности быть одновременно в любой точке пространства, электроны при заполнении орбиталей соблюдают определенный порядок:
У этого правила есть еще одно мнемоническое название — правило троллейбуса. Расположение электронов напоминает рассадку в общественном транспорте. Если есть свободные места и человек входит один, он сядет на свободное сиденье, и только если нет свободных сидений, подсядет к кому-то на свободное место.
Итак, подведем выводы, на которые ученым понадобилось более сотни лет опытов, исследований, научных дискуссий и даже трагедий.
Чтобы проверить насколько хорошо усвоен материал, предлагаем вашему вниманию тест на тему «Строение атома» для 8-11 классов:
Строение атома. Гибридизация орбиталей
Обычно в начале статьи пишут краткий план того, о чем пойдет речь в статье. Еще добавляют зачем и почему на нее нужно тратить время. Но здесь такого не будет, потому что я не уверен — нужна ли она вообще.
Но я расскажу историю. Вообще статья должна была быть про белок, как формируется первичная, вторичная структура, ну и так далее. И вот идет подготовка материала, а там довольно большую роль играет электроотрицательность. На самом деле не очень и большую, но все-таки роль у нее есть. И вот мне стало интересно, а как она формируется? Ты конечно знаешь, что она растет в периодической таблице слева направо и зависит от радиуса атома. Но почему? В общем-то эти вопросы привели меня к строению атома и закону Кулона. Поэтому сейчас мы устроим маленькое путешествие в химию и физику. Начнем со строения атома. А уже в следующей статье будем разбираться с электроотрицательностью.
Планетарная модель строения атома от Резерфорда
Это модель ключевая, потому что на ее основе строились все остальные. Вообще Резерфорд крутой мужик, который очень любил всякие опыты. Вот один из них:
Какие выводы делает Резерфорд из этого опыта? Он предполагает, что основная масса атома сосредоточена в его ядре — когда альфа-частицы попадают в него, то отскакивают в обратную сторону. Ядро очень маленькое и заряжено положительно, а вокруг него по орбитам летают отрицательно заряженные электроны. Он называет это планетарной моделью. Очень красиво, согласитесь? Мы живем в мире, который находится в солнечной системе. А атомы, из которых состоит все вокруг, имеют строение такой же системы.
Это все очень поэтично и красиво, но есть парочка проблем:
Были и еще проблемы, но это основные. Как же их решить?
Полуклассическая модель атома по Бору
Появляется второй крутой мужик. Может быть, он даже круче первого, потому что говорит такое — от чего волосы у физиков встают дыбом. Бор взял модель атома по Резерфорду и сказал что-то вроде: «Давайте предположим, что электроны движутся по орбитам, но никакую энергию они не излучают. Но если электрон перепрыгивает с одной орбиты на другую, то он выделяет энергию — фотоны. Это и есть спектр!»
Бор назвал состояние атома, когда его электроны движутся по свои орбитам, стационарным состоянием. При перепрыгивании одного электрона на другую орбиту атом становится возбужденным и может выделять энергию. Атом становится возбужденным не просто так — он поглощает какую-то энергию извне, она представляет собой фотон или фотоны.
Переведем Бора на язык физиков: “Вся ваша физика полная туфта. Атому на нее плевать, он живет по другим законам”. И все как бы в шоке, но больше всех Эйнштейн — он становится главным хейтером Бора. Но экспериментально модель Бора подтверждается.
Модель Бора чем-то похожа на дом. Представьте себе панельку. Если электрон упадет с 7 этажа на первый, то он выделит энергию — это и есть фотон. А вот если зарядить как следует атом, то электрон может прыгнуть с первого этажа на пятый. Чем больше зарядишь, тем выше прыгнет. Чем с большей высоты упадет, тем больше выделит энергии. Примерно так. Оказалось, что Бор был прав и дальше мы это увидим.
Резерфорд, кстати, сделал предположение, что ядро состоит из положительно заряженных протонов. Но Резерфорд и Бор еще не знали, от чего зависит количество электронов и протонов, но с этим разберутся попозже.
Современная модель атома
Ну а дальше началось самое интересное — физики взяли модель атома по Бору и добавили к ней своего добра. Так получилась современная модель атома. Конец! Ну или не совсем. Атом состоит из ядра и электронной оболочки. Начинаем с ядра.
Ядро атома
У атома есть ядро, которое состоит из протонов и нейтронов. Протоны заряжены положительно, а у нейтронов заряда нет. Количество протонов и электронов равно — зависит от порядкового номера в таблице Менделеева. Если это атом азота, то у него 7 протонов и 7 электронов. Нейтрон такому правилу не подчиняется — их может быть больше, а может и меньше. Протон и нейтрон весят в примерно 1800 раз больше, чем электрон. Поэтому основная масса атома находится в ядре.
На самом деле протон и нейтрон состоят из других частиц, но не будем слишком глубоко копать. Можешь почитать, если интересно.
Электронная оболочка
Электронная оболочка — это все электроны атома. Она состоит из слоев, на которых располагается какая-то часть электронов.
Каждый слой состоит из орбиталей. Заметили? Не орбит, а орбиталей. Орбита — это траектория движения тела, на которой в какой-то момент времени можно его встретить. Помните круговые поливалки в деревне? Вода из них движется по определенной траектории. Можно встать и подождать пока тебя польют в жаркий день. Орбиталь — это другое дело, на ней электрон проводит 90 процентов времени, но как он там движется — одному ему известно. Поэтому можно стоять очень долго, но так и не дождаться пока тебя польют. Пример не очень, согласен. Лучше бы привел Луну или какую-нибудь планету, но вы поняли…
Есть 4 вида орбиталей: s, p, d и f. S- это сфера, p — бесконечность или гантелька, d и f сложнее. Я их рисовать не буду, потому что они нас не интересуют. P-орбиталей всегда 3 — px, py, pz.
Слои электронной оболочки
Теперь подробнее про слои. Первый слой состоит только из одной орбитали — s. Второй слой: одна s и три p орбиталей. Третий слой — одна s, три p и пять d орбиталей. Ну а на четвертом за 5d орбиталями добавятся еще 7f. Количество слоев зависит от количества электронов, а значит от порядкового номера атома.
Тут есть определенные правила:
Добавим к атому лития, который я показывал до этого, орбитали и получим что-то такое.
Можно еще попробовать свести орбитали в один рисунок, смотрите.
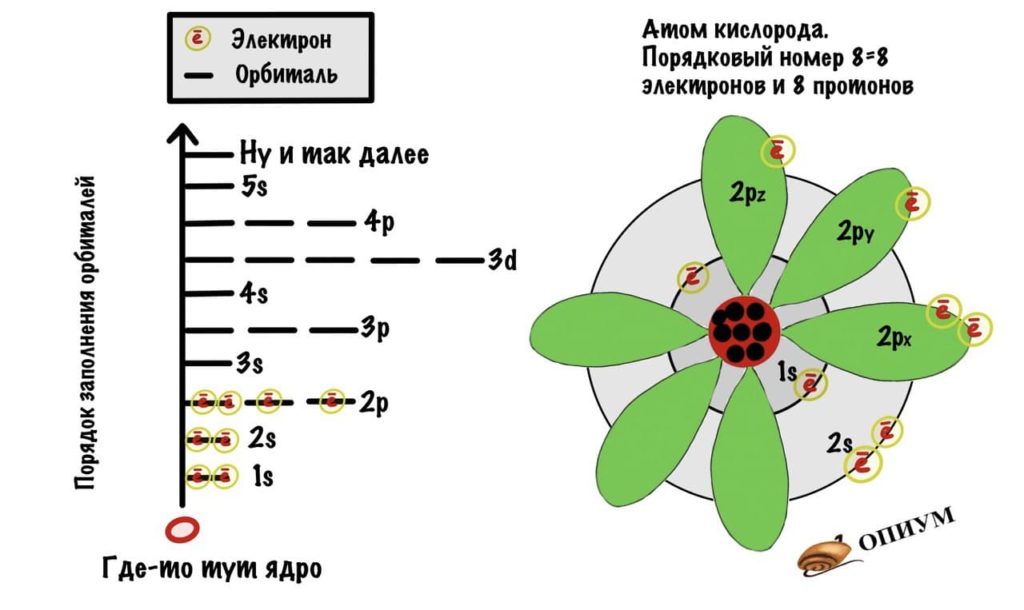
Химические связи чаще всего образуются за счет неспаренных электронов, но подробнее об этом поговорим в следующей статье. А сейчас нас интересует углерод и гибридизация его орбиталей.
Гибридизация орбиталей
Сначала посмотрим на электронную формулу углерода и вспомним о Боре. В стационарном состоянии у углерода всего два электрона на 2p-орбиталях. Однако, если атом углерода поглотит энергию фотона, то электрон с 2s-орбитали может перейти на 2p-орбиталь — атом углерода становится возбужденным. В таком состоянии он может образовать 4 связи, т.к. у него 4 неспаренных электрона.
И тут встал вопрос. Атом углерода в возбужденном состоянии может образовать четыре связи, так как у него четыре неспаренных электрона. Но энергия связей будет разной, потому что эти электроны располагаются на разных орбиталях (у p орбитали энергия побольше). Это не очень хорошо сказывается на стабильности системы. Как выйти из этого положения? Атом придумал интересную штуку — он изменил форму и размеры орбиталей. Это и есть гибридизация.
У азота есть одна неподеленная электронная пара на втором энергетическом слое, а именно на 2s-орбитали — там находится два электрона и третий туда уже не засунуть. Но азот может отдать протону водорода один электрон по донорно-акцептерному механизму и образовать связь. Так возникает ион аммония. Такая же тема с водой, но кислород не может отдать по электрону от каждой электронной пары — только с одной! Так образуется ион гидроксония.
sp 2 и sp-гибридизация
Куда пропала p-связь? Ну ладно, держите формулу этилена со всеми связями.
На рисунке видно, что p-орбитали без гибридизации находятся над и под плоскостью, они образуют сигма-связь — эта связь более жесткая, чем пи-связь. Поэтому вращение вокруг нее ограничено.
sp-гибридизацию нарисовать не смогу, сорян. Но смысл вы поняли: без изменений останутся две p-орбитали, а две sp-орбитали будут похожи на палочку — угол между ними будет 180 градусов. Одна p-орбиталь будет идти над плоскостью, а другая смотреть в лицо. Надеюсь, что у тебя получилось представить. Едем дальше.
Атомный остов
Электронный слой бывает завершенным или незавершенным:
Заряд ядра атома (количество протонов) + заряд завершенных слоев (количество электронов) = атомный остов. Картинка….
У кислорода заряд атомного остова больше, чем у натрия. Это нам понадобится, когда будем считать электроотрицательность.
Фух, со строением атома закончили. Поздравляю всех, кто дочитал до этого момента. Дальше можно переходить к электроотрицательности, но это уже в следующей статье.
Хочешь задать вопрос, похвалить или наговорить гадостей? Тогда залетай в телегу. Там ты сможешь предложить новый формат или разбор темы. А если серьёзно, то эти статьи пишутся для вас, поэтому мне важна обратная связь.